Guia de laboratorio de QuÃmica I 2018.pdf
Vista previa de texto
Prof. Jesús Rivero Lacruz. Guía Didáctica computarizada de Prácticas de Laboratorio de Química I
*
Conversión
Unidades de:
de En unidades de
Fórmula
conversión
de Significado de términos
-
+ ,
Molaridad (M)
Normalidad (N)
Normalidad (N) = n = (OH , H
Molaridad x n
Oxidación)
Molaridad (M)
Molalidad (m)
Molalidad=
Molaridad /d
Normalidad (N)
Molaridad (M)
Molaridad
Normalidad / n
Normalidad (N)
Molalidad (m)
Molalidad=
n = (OH , H
Normalidad / n x Oxidación)
d
Nº. total de estado de
densidad del disolvente (Kg/L)
-
+ ,
Nº. total de estado de
-
+ ,
Nº. total de estado de
= n = (OH , H
Oxidación)
d = densidad del disolvente (Kg/L)
Molalidad (m)
Molaridad (M)
Molaridad=
Molalidad x d
densidad del disolvente (Kg/L)
Molalidad (m)
Normalidad (N)
Normalidad=
n = (OH , H
Molalidad x d x n Oxidación)
-
+ ,
Nº. total de estado de
densidad del disolvente (Kg/L)
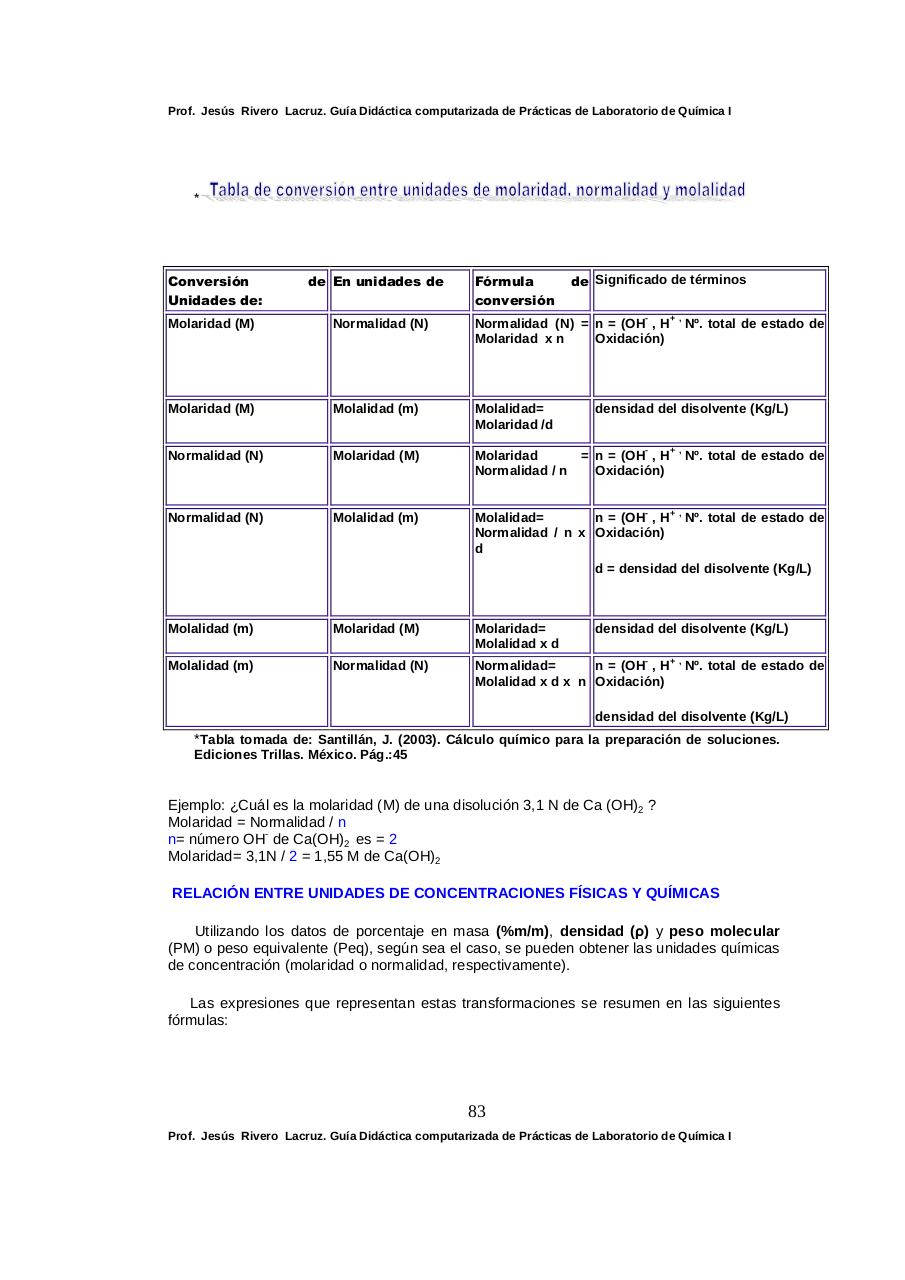
*Tabla tomada de: Santillán, J. (2003). Cálculo químico para la preparación de soluciones.
Ediciones Trillas. México. Pág.:45
Ejemplo: ¿Cuál es la molaridad (M) de una disolución 3,1 N de Ca (OH)2 ?
Molaridad = Normalidad / n
n= número OH de Ca(OH)2 es = 2
Molaridad= 3,1N / 2 = 1,55 M de Ca(OH)2
RELACIÓN ENTRE UNIDADES DE CONCENTRACIONES FÍSICAS Y QUÍMICAS
Utilizando los datos de porcentaje en masa (%m/m), densidad (ρ) y peso molecular
(PM) o peso equivalente (Peq), según sea el caso, se pueden obtener las unidades químicas
de concentración (molaridad o normalidad, respectivamente).
Las expresiones que representan estas transformaciones se resumen en las siguientes
fórmulas:
83
Prof. Jesús Rivero Lacruz. Guía Didáctica computarizada de Prácticas de Laboratorio de Química I
