Guia de laboratorio de QuÃmica I 2018.pdf
Vista previa de texto
Prof. Jesús Rivero Lacruz. Guía Didáctica computarizada de Prácticas de Laboratorio de Química I
Tabla 5.1
Tipo de disolución
Algunos Ejemplos Disolvente
Soluto
GAS
Aire
Nitrógeno
(gas)
Gas en líquido
Agua
Carbonatada
Líquido en líquido
Sólido en líquido
Gas en gas
N2
Oxígeno (O2 )
(gas)
Agua (líquido)
Dióxido de carbono (CO2)
(gas)
Vinagre
Agua (líquido)
Ácido acético
(Líquido)
Agua de mar
Agua (líquido)
Cloruro de sodio (NaCl)
( sólido)
Líquido en sólido
Amalgama
Plata (sólido)
Mercurio (Hg)
(Líquido)
Sólido en sólido
Acero
Hierro (sólido)
Carbono
(sólido)
Líquido
Sólidos
CONCENTRACIONES DE DISOLUCIONES
La concentración es una unidad de medición general que indica la cantidad de soluto
presente en una cantidad conocida de disolución o disolvente. La concentración de una
disolución depende de la relación entre la cantidad de soluto y disolvente presente en ella.
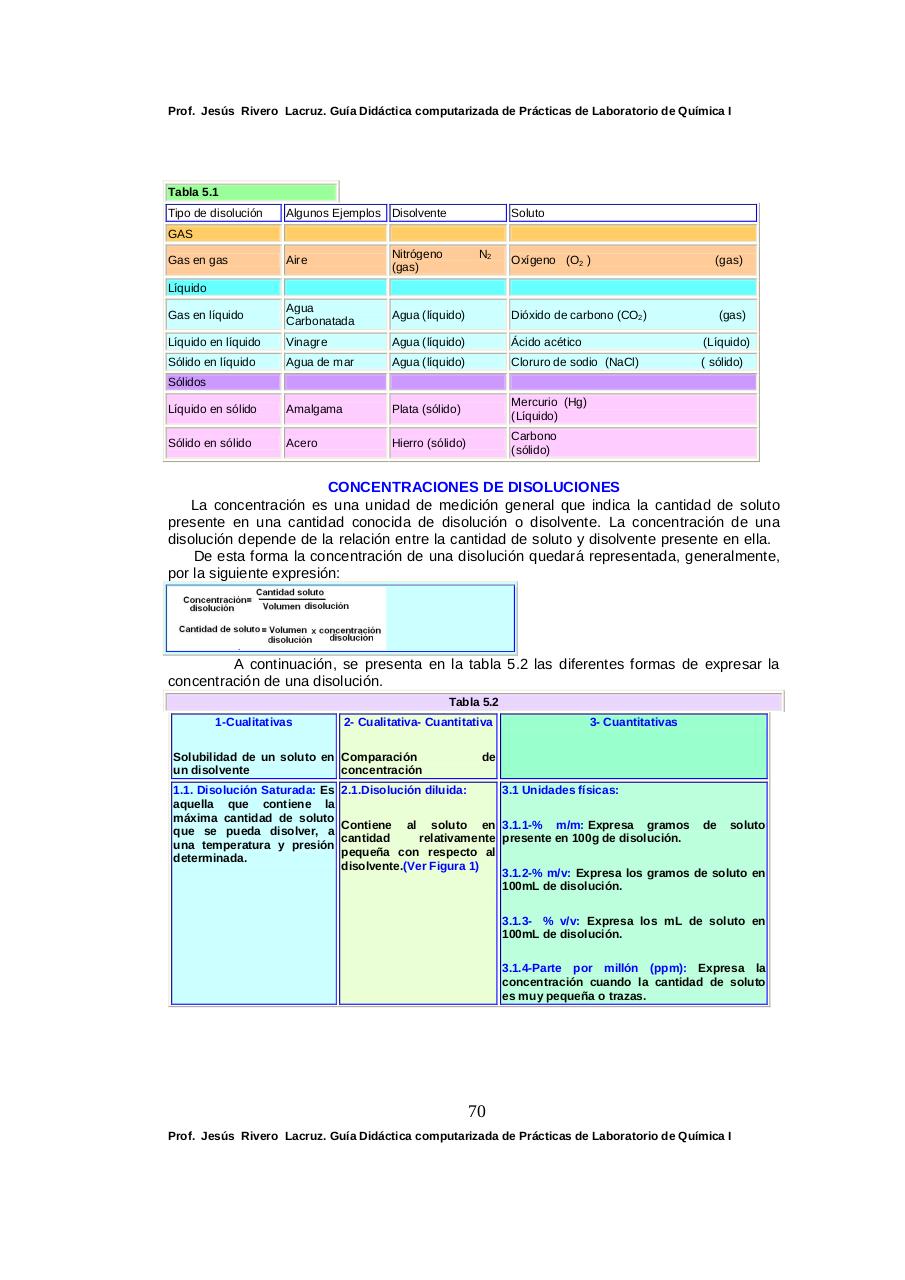
De esta forma la concentración de una disolución quedará representada, generalmente,
por la siguiente expresión:
A continuación, se presenta en la tabla 5.2 las diferentes formas de expresar la
concentración de una disolución.
Tabla 5.2
1-Cualitativas
2- Cualitativa- Cuantitativa
Solubilidad de un soluto en Comparación
un disolvente
concentración
1.1. Disolución Saturada: Es
aquella que contiene la
máxima cantidad de soluto
que se pueda disolver, a
una temperatura y presión
determinada.
3- Cuantitativas
de
2.1.Disolución diluida:
3.1 Unidades físicas:
Contiene al soluto en 3.1.1-% m/m: Expresa gramos de soluto
cantidad
relativamente presente en 100g de disolución.
pequeña con respecto al
disolvente.(Ver Figura 1)
3.1.2-% m/v: Expresa los gramos de soluto en
100mL de disolución.
3.1.3- % v/v: Expresa los mL de soluto en
100mL de disolución.
3.1.4-Parte por millón (ppm): Expresa la
concentración cuando la cantidad de soluto
es muy pequeña o trazas.
70
Prof. Jesús Rivero Lacruz. Guía Didáctica computarizada de Prácticas de Laboratorio de Química I
